综述设计用于细胞治疗的药物递送系统
自体细胞治疗的挑战
尽管在细胞疗法的开发方面取得了重大进展,但一系列共同的挑战依然存在。例如,基于T细胞的疗法,如嵌合抗原受体(CAR)-T细胞疗法,在治疗某些血液癌症方面已显示出临床成功。然而,它们的有效性和安全性应进一步提高,特别是注入的T细胞的持久性和功能性有限。调节性T(Treg)细胞因其能够调节免疫系统的能力,正在被探索用于治疗自身免疫性疾病并预防器官移植排斥。然而,精确操纵它们并确保其在患者体内的持续存在和功能仍然具有挑战性。自然杀伤细胞是先天免疫系统的一部分,能够在没有先前致敏的情况下消除癌细胞和病毒感染细胞。因此,已经研究了自然杀伤细胞来治疗癌症,其优势是不会引起与CAR-T细胞疗法相关的严重副作用。尽管如此,与T细胞类似,有效地在体外扩增自然杀伤细胞并在体内保持其治疗功能仍然很困难。此外,自然杀伤细胞治疗需要全身给药刺激性细胞因子。基于巨噬细胞的疗法在组织修复和癌症治疗中显示出潜力,但在治疗环境中控制巨噬细胞极化和行为仍然复杂,担心意外后果,如促进肿瘤生长或加剧炎症反应。
细胞治疗的药物递送平台
药物递送技术可以应用于增强细胞疗法的有效性,通过微调治疗性细胞的生物功能、保护它们免受潜在伤害,并扩展它们作为针对性递送导航器的用途。在基于T细胞的疗法方面,药物递送系统可以调节细胞运输、遗传修饰T细胞、增强T细胞激活和耐力,并使T细胞能够运送至受影响部位以重塑疾病微环境。此外,药物递送系统可以通过增强细胞激活(无需共给药刺激性细胞因子)以及提高自然杀伤细胞在体外扩增的效率来增强自然杀伤细胞疗法。药物递送系统还可以调节释放免疫调节因子,以引导巨噬细胞极化朝向期望的表型和功能,同时最小化不良炎症反应或组织损伤。由于巨噬细胞具有固有的归巢能力,可克服体内的生物屏障,因此也可以作为靶向递送的载体。红细胞(RBCs),在治疗血液学疾病方面有着悠久的历史,可以与药物递送系统集成用于组织特异性药物递送,这种方法已达到临床应用。此外,对于干细胞移植和β细胞疗法,药物递送系统可以创造保护性微环境,保护移植细胞免受宿主免疫系统的伤害,并促进提供必要的生物分子,确保这些细胞的长期存活和最佳功能。
调节细胞功能的药物递送系统
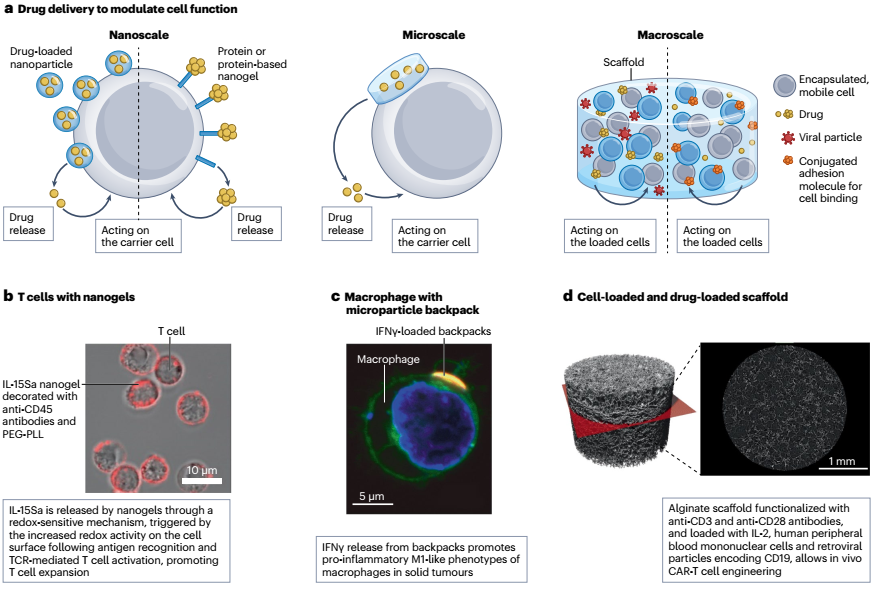
细胞因子通常通过与治疗性细胞共同给药来增强细胞潜能;然而,系统性细胞因子递送可能会引起不良效应。刺激响应性“无载体”蛋白质纳米凝胶可以解决这些缺点;例如,通过二硫键含有的双N-羟基琥珀酰亚胺(NHS)交联剂(NHS-SS-NHS)交联IL-15Sa蛋白合成的纳米凝胶可以用抗CD45抗体和聚乙二醇-b-聚(L-赖氨酸)(PEG-PLL)装饰,然后与pmel-1 CD8+ T细胞结合(图1b)。抗CD45涂层允许与T细胞上的特定配体结合,并将纳米凝胶保留在细胞表面。此外,PEG-PLL促进了与细胞的静电关联。值得注意的是,还允许纳米凝胶附着到细胞表面的硫醇-马来酰亚胺点击反应,导致纳米凝胶通过细胞表面细胞因子受体快速内化到细胞中;因此,这种化学方法没有被用于纳米凝胶的结合。研究表明:通过氧化还原敏感机制实现组织特异性释放IL-15Sa,该机制由抗原识别后细胞表面增加的氧化还原活性触发,以及在小鼠黑色素瘤模型中的肿瘤和肿瘤引流淋巴结中T细胞受体(TCR)介导的T细胞激活。重要的是,这种方法使得细胞因子的安全递送剂量至少比通过游离细胞因子注射可实现的剂量高出八倍,而不会引起毒性。
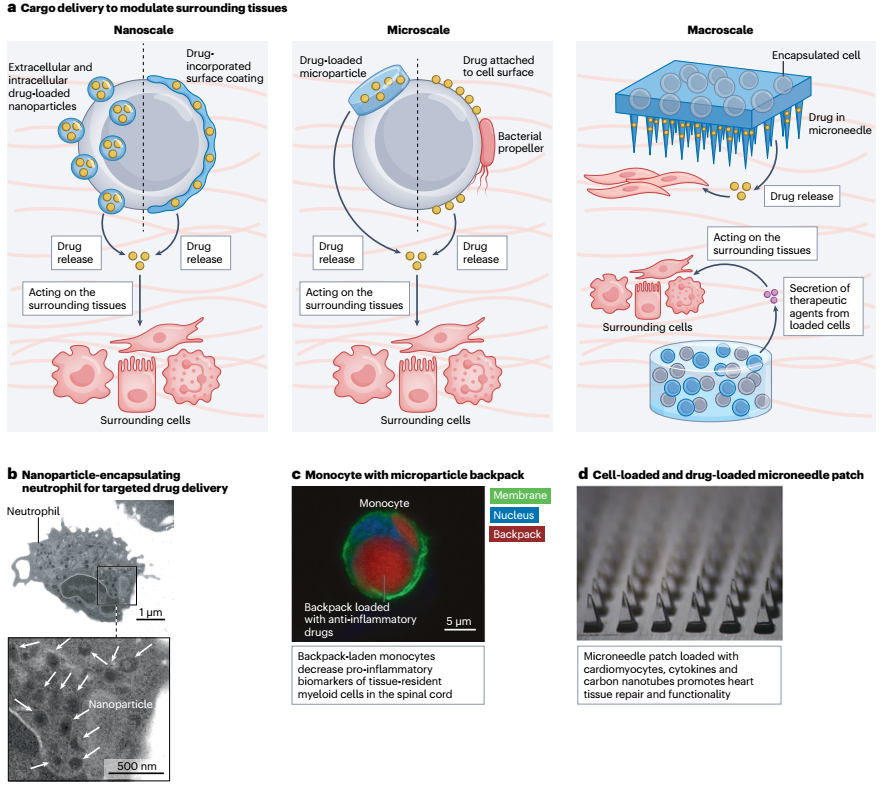
调节周围组织的药物递送
保护体内治疗性细胞
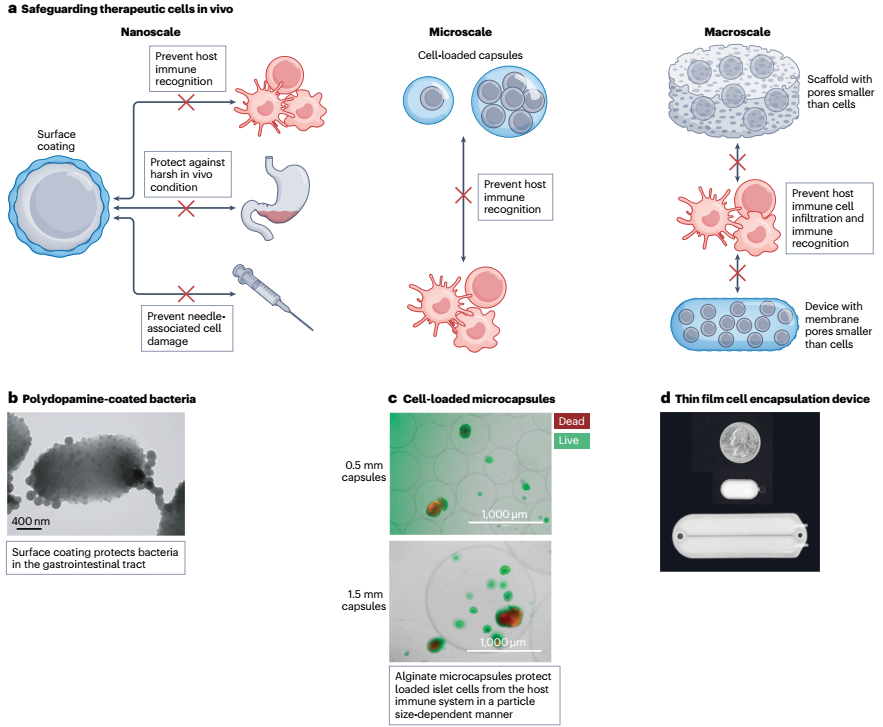
细胞疗法的有效性可能会受到环境影响、宿主识别以及随后的异物反应的损害。生物材料可以用来保护治疗性细胞免受化学和生物化学环境的影响,避免免疫细胞的识别和清除,并维持它们的活力和功能(图3a)。细胞可以用聚合物或纳米材料涂覆,以形成保护层,提高它们的存活率和效能。聚合物和纳米材料可以直接嫁接到细胞表面,或者通过原位聚合和交联实现。直接接枝可以通过与固有的胺基和硫醇基团进行共价反应来实现,或者通过在细胞膜上添加非天然官能团(例如,酮和叠氮化物)来实现。另外,非共价相互作用(如氢键和脂质或烷基链的细胞膜插入)也允许直接接枝。这些策略可以应用于将材料稳定地附着到细胞表面,以保护细胞免受环境损害,并防止它们的免疫识别和排斥。例如,通过氰尿酰氯偶联将甲氧基聚乙二醇(mPEG)修饰到红细胞(RBC)表面,可以掩盖RBC的表面抗原,并促进异种细胞的存活。此外,灵活且水合的mPEG链在细胞周围形成立体排除体积,阻止生物大分子(如抗体)和其他细胞的结合。mPEG涂覆的RBCs进一步减少了它们的聚集和主要(ABO)及次要(Rh和MNS)抗原的反应性,同时不影响RBCs的形态、结构和功能。此外,经mPEG修饰的绵羊RBCs在被人外周血单核细胞吞噬方面表现出显著减少的现象,并且当输给小鼠时,与未经修饰的RBCs相比,它们的生存时间提高了360倍。
原位聚合和交联使得能够在细胞表面固定聚合物网络,这可以作为保护层来保护细胞免受微环境和宿主免疫系统的影响。例如,胃肠道中的条件,如胃液、胆盐和消化酶的存在,可能会对口服给药后的益生菌的存活率产生负面影响。通过在细胞兼容条件下在细菌表面聚合多巴胺,以及共沉积功能分子(图3b),可以保护细菌。聚多巴胺表面修饰显著提高了封装细胞对胃酸和胆盐的抵抗力,促进了它们在小鼠胃和肠道中的生存。此外,它们增强的口服生物利用度和在炎症肠组织的积累提高了它们在小鼠结肠炎模型中的治疗效果,超过了一线药物氨基水杨酸的效果。而且,神经干细胞(NSCs)可以通过生物启发的矿化作用涂覆氢键有机框架,以保持NSC干性和防止注射器针头造成的细胞膜损伤。然而,原位聚合和交联方法需要与活细胞兼容的制造方法,这限制了材料选择。此外,纳米级壳层的形成,特别是不可降解涂层,可能会阻碍细胞分裂。
总结与展望

