揭秘AAV:高分辨率冷冻电镜表征AAV载体结构
rAAV空壳病毒的产生与影响
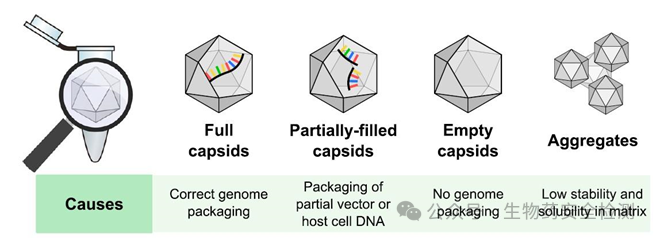
在rAAV的生产过程中,病毒基因组进入细胞核中进行复制,经转录、翻译得到衣壳蛋白,并进行组装,随后在解旋酶复合物的介导下,核酸被引导并组装进入衣壳中,最终组装成完整的病毒颗粒(Full)。但在实际生产中,会产生多种类型的病毒颗粒,如完整病毒(衣壳中有完整的基因组)、部分包装病毒(包装了部分正确的DNA片段或者错误的DNA片段)、空壳病毒(衣壳内部没有DNA或者只有一些很小的DNA片段)、病毒聚集体、破损病毒等(见图1)[2] 。研究表明,这些空壳病毒和部分包装病毒会影响终产品的纯度,并可能降低病毒的转导效率,引发不必要的免疫反应,增加总体病毒载量[3] 。因此监管机构要求在整个生产过程中监控各类产品相关杂质,尤其是空壳AAV的比率。
rAAV载体空壳率的质控检测方法简介
-
沉降系数只是颗粒的一个属性,不等同于颗粒类型,不同颗粒类型的沉降系数可能非常接近。例如在AUC检测中,完整病毒颗粒特征峰所对应的颗粒群体中可能包括多种颗粒类型,如真正的无损伤的完整病毒颗粒、局部变形的完整病毒颗粒、有一定破损的完整病毒颗粒、一定程度的寡聚物(如病毒碎片,或者病毒碎片与空壳颗粒形成的寡聚体),或其他质量和密度类似的杂质颗粒;
-
对样品要求较高,只能用于纯化样品的检测,样品浓度需高达5x10^12 VP/mL,样本量需500uL左右;
-
长时间离心过程中的机械剪切力可能会影响病毒结构,造成病毒颗粒变形、破损、聚集等,影响检测结果;
-
AUC检测无法区分病毒聚集体中的空壳和实心颗粒,也无法区分一定程度的破损颗粒和空壳颗粒,及破损的完整病毒颗粒和无破损的完整病毒颗粒;
-
检测通量较低,单次运行约6个小时,分析3-7个样本,数据分析时间较长;
-
在GMP环境中实施AUC检测,需慎重评估离心过程中气溶胶带来的风险。
高分辨率冷冻电镜检测技术
实现单次表征多种属性

